 Ayer miércoles, 13 de abril de 2016 arrancó la 51 edición del Encuentro Anual de la Asociación Europea para el Estudio del Hígado (EASL 2016) en la ciudad de Barcelona, que se prolongará hasta el día 17. Este encuentro (el Congreso Internacional del Hígado) es una de las principales citas anuales para exponer los avances científicos en torno a las hepatitis víricas, sus tratamientos y complicaciones, así como otros temas relacionados con la salud hepática.
Ayer miércoles, 13 de abril de 2016 arrancó la 51 edición del Encuentro Anual de la Asociación Europea para el Estudio del Hígado (EASL 2016) en la ciudad de Barcelona, que se prolongará hasta el día 17. Este encuentro (el Congreso Internacional del Hígado) es una de las principales citas anuales para exponer los avances científicos en torno a las hepatitis víricas, sus tratamientos y complicaciones, así como otros temas relacionados con la salud hepática.
Por poner cifras al problema de salud que suponen las enfermedades del hígado, se calcula que solo en Europa, la cirrosis es la causa de 170.000 fallecimientos al año (aproximadamente el 2% del total de muertes anuales). Por su parte, el cáncer hepático es la segunda causa de muerte por cáncer en el mundo y, cada año, entre 350.000 y 500.000 personas fallecen debido a problemas relacionados con la hepatitis C en el mundo. 
Precisamente el ámbito del tratamiento de la hepatitis C sufrió un cambio de paradigma a raíz de la introducción de los fármacos de acción directa (DAA, en sus siglas en inglés), que actúan directamente en el ciclo de replicación del virus de la hepatitis C (VHC), alcanzando cotas de curación que en muchas ocasiones se aproximan al 100%. En esta edición de la conferencia se espera que se expongan novedades dirigidas a optimizar esta terapia, así como resultados en entornos reales de las intervenciones realizadas.
Así, se presentarán resultados de estudios en los que se ha probado la combinación sofosbuvir (Sovaldi®) y velpatasvir (un inhibidor del complejo de replicación NS5A, de acción pangenotípica) [véase La Noticia del Día 02/11/2015], los fármacos experimentales ABT-493 y ABT-530 o la coformulación grazoprevir/elbasvir (Zepatier®) [véase La Noticia del Día 02/12/2015].
En el congreso también se expondrán novedades relacionadas con las nuevas terapias para tratar la hepatitis B, la esteatosis hepática o el manejo de complicaciones hepáticas tales como cirrosis, cáncer de hígado o los trasplantes, entre otros temas.
En el transcurso de la ceremonia inaugural, representantes de las principales organizaciones en el campo de las enfermedades hepáticas firmaron una declaración conjunta para la eliminación de las hepatitis virales, en donde se insta a los gobiernos, organizaciones de la salud y a las ONG a implementar los siguientes planes de acción: a reconocer la carga sobre la salud pública que suponen las hepatitis víricas y establecer estrategias para frenar su impacto; a implantar las infraestructuras de tomas de datos necesarias para valorar el impacto de las hepatitis víricas sobre la salud pública; a establecer directrices prácticas en las que se incluyan recomendaciones sobre inmunización, cribado, diagnóstico y tratamiento; a desarrollar e implementar planes integrales de prevención de la hepatitis; a identificar a las poblaciones en situación de mayor riesgo para realizar el cribado de hepatitis B y C; a hacer que estén disponibles unas pruebas de cribado y diagnóstico baratas y precsas en los programas de salud pública; a implementar y financiar los programas sanitarios para diagnosticar y tratar a las personas con infeción crónica con el objetvo de minimizar y, con el tiempo, el eliminar la carga para la salud que suponen las hepatitis víricas y a apoyar la realización de más estudios.
Puedes encontrar la declaración conjunta en este enlace.
Excelentes resultados de sofosbuvir, velpatasvir y GS-9857 en personas con fracaso previo a antivirales de acción directa
En el Congreso Internacional del Hígado se han presentado los resultados conjuntos de dos estudios que evaluaron el uso de la combinación formada por sofosbuvir (Sovaldi®, también en Harvoni®) y los fármacos en investigación velpatasvir (un inhibidor del complejo de replicación NS5a) y GS-9857 (un inhibidor de la proteasa NS3/4A pangenotípico) en el tratamiento de personas con el virus de la hepatitis C (VHC) de cualquier genotipo que habían fracasado a uno o varios tratamientos previos. Algunos de los participantes habían realizado tratamientos con uno o varios fármacos de acción directa.
Los dos estudios de fase II, GS-US-367-1168 y GS-US-367-1169, investigaron la eficacia y la tolerabilidad de un tratamiento de 12 semanas con una administración diaria de la píldora combinada sofosbuvir/velpatasvir (400 y 100mg, respectivamente) y de GS-9857 (100mg).
Un total de 128 participantes fueron incluidos en esta revisión conjunta. El 49% tenían genotipo 1, el 16% genotipo 2, el 27% genotipo 3, el 5% genotipo 4 y el 2% genotipo 6. El 75% eran hombres, el 82% de etnia blanca, el 73% tenía genotipo desfavorable de la interleuquina 28B (IL-28B) y el 48% tenía cirrosis hepática.
La experiencia previa en tratamientos se resume en la siguiente tabla:
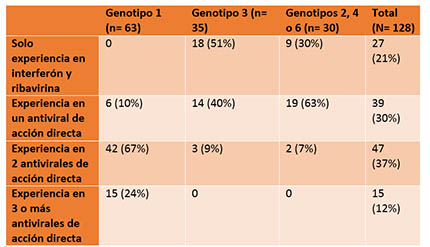
Al entrar en el estudio, el 60% de los participantes tenía VHC con variantes genotípicas asociadas a resistencia (el 20% en el complejo de replicación NS5a, el 15% en la proteasa NS3 y un 2% en la polimerasa NS5B.
El 99% de los participantes obtuvo respuesta virológica sostenida a las 12 semanas de finalizar el tratamiento (RVS12, en la práctica clínica sinónimo de curación). Solo una persona –que experimentó recidiva, es decir, rebrote virológico tras finalizar el tratamiento indetectable- no logró la curación. Dicha persona, al entrar en el estudio, tenía cirrosis hepática y la variante Y93H del complejo de replicación NS5a –asociada a resistencia-. Tras la recidiva se hallaron variantes asociadas a resistencia del complejo de replicación NS5a, de la proteasa NS3 y de la polimerasa NS5B.
Los efectos secundarios más frecuentes –que sucedieron en más del 10% de los participantes- fueron dolor de cabeza, fatiga, diarrea y náuseas. En la mayor parte de los casos fueron de intensidad leve o moderada.
Un participante experimentó un efecto secundario de intensidad grave (gastroenteritis) y uno abandonó el tratamiento a la semana 9 por causa de un episodio de gastritis (aunque finalmente alcanzó RVS12). Ambos efectos secundarios no fueron considerados vinculados al tratamiento por parte de los investigadores. Durante el estudio no se observaron alteraciones en los valores de laboratorio de las analíticas de seguimiento.
Los resultados del presente estudio muestran que la combinación formada por sofosbuvir/velpatasvir y GS-9857, tomada durante 12 semanas, sería una opción terapéutica segura y altamente eficaz para personas con VHC de cualquier genotipo tras un fracaso previo con cualquiera de los tratamientos contra el VHC existentes.
Fuente: Elaboración propia (gTt-VIH)
Referencias: EASL. International Liver Congress (http://ilc-congress.eu/)
Lawitz E, Kowdley K, Curry M, et al. High efficacy of sofosbuvir/velpatasvir plus gs-9857 for 12 weeks in treatment-experienced genotype 1-6 hcv-infected patients, including those previously treated with direct-acting antivirals. 2016 International Liver Congress: 51th Annual Meeting of the European Association for the Study of the Liver (EASL). Barcelona, April 23-27, 2015. Abstract PS008.
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.







