El Grupo de Trabajo sobre Tratamientos del VIH (gTt) os ofrece una cobertura informativa especial de la XVII Conferencia Internacional sobre el Sida desde la sede de la conferencia en Ciudad de México. Durante toda la semana, del 4 al 8 de agosto, se publicarán boletines diarios de noticias sobre los aspectos más destacados de esta conferencia, que podrán consultarse a diario en www.gtt-vih.org, o recibirse vía e-mail o RSS
•Posible interacción entre raltegravir y tipranavir
•Recidiva del VHC en personas que consiguieron eliminar el virus al final del tratamiento
•Coinfección y riesgo de infarto agudo de miocardio y enfermedad cerebrovascular
•Darunavir/r tiene un impacto menor sobre los lípidos que lopinavir/r
•Un estudio sobre monoterapia con lopinavir/r muestra altas tasas de fracaso no esperadas
Posible interacción entre raltegravir y tipranavir
Juanse Hernández
Un estudio presentado en la Conferencia de México ha mostrado que substituir el inhibidor de la fusión enfuvirtida (T20, Fuzeon®) por el inhibidor de la integrasa raltegravir causó aparentemente citólisis hepática, o lo que es lo mismo una destrucción de las células hepáticas, en tres personas que estaban tomando un régimen antirretroviral que incluía el inhibidor de la proteasa tipranavir (Aptivus®). En una de las personas se midieron los niveles valle de tipranavir antes y después de producirse el cambio a raltegravir y los resultados muestran que el inhibidor de la integrasa podría potenciar las concentraciones de tipranavir hasta un nivel de riesgo de toxicidad.
El hallazgo es particularmente importante dado que, desde que raltegravir está disponible en los hospitales, muchas personas que estaban tomando enfuvirtida han decidido junto a sus médicos cambiarlo por raltegravir como consecuencia de la dificultad de administrar el inhibidor de la fusión y por las reacciones que provoca en la zona de inyección.
Es bien sabido que la toxicidad hepática de tipranavir limita su uso a personas que no padecen enfermedades hepáticas. Sin embargo, hasta la fecha, poco se sabe sobre las posibles interacciones entre tipranavir y raltegravir. Ahora, un grupo de médicos de la AIDS Healthcare Foundation en Los Ángeles (EE UU) y de la Universidad de Nantes (Francia) han hallado tres casos de citólisis hepática en tres hombres que cambiaron enfuvirtida por raltegravir. Hasta la fecha, el inhibidor de la integrasa ha mostrado un perfil de seguridad muy favorable.
El promedio de edad de los tres pacientes fue de 50 años (rango 40-70), y la media del recuento de linfocitos CD4 antes de iniciar raltegravir fue de 377 células/mm3 (rango 132-544). Los tres individuos tenían carga viral indetectable y ninguno había desarrollado citolisis hepática previamente.
Además de tipranavir y ritonavir, dos de los hombres estaban tomando tenofovir (Viread®) y emtricitabina (Emtriva®) y el tercero, tenofovir, zidovudina, lamivudina y abacavir. A los pacientes se les realizó varias pruebas para detectar la presencia de hepatitis virales, pero no revelaron nada. Ninguno de los tres estaba tomando otros medicamentos hepatotóxicos.
En el plazo de dos a cuatro semanas de cambiar a raltegravir, los niveles de la enzima hépatica aspartato aminotransferasa (AST) de los tres hombres aumentaron entre 4 y 10 veces el límite normal superior; y los de alanino aminotransferasa (ALT), 4 y 40 veces el límite normal superior.
En un paciente, los médicos midieron los niveles valle de tipranavir antes y después de iniciar raltegravir y observaron que las concentraciones aumentaron de 46 a 108ng/mL, un incremento muy por encima del rango terapéutico de tipranavir/ritonavir, que se sitúa entre 10 y 39ng/mL .
Como consecuencia, dos hombres cambiaron tipranavir por darunavir (Prezista®), y las enzimas AST y ALT volvieron a los niveles normales. El tercero continuó tomando tipranavir porque sus niveles de enzimas hepáticas descendieron a 2 veces el límite normal superior y la concentración valle de tipranavir fue de 40ng/mL.
En sus conclusiones, los médicos sugieren que una posible interacción entre raltegravir y tipranavir podría explicar el aumento de los marcadores de la función hepática tras el cambio de fármaco y recomiendan utilizar raltegravir con precaución en personas que toman tipranavir hasta que se disponga de más datos sobre las interacciones entre ambos fármacos.
Fuente: Elaboración propia / Natap.
Referencia: Khanlou H, Allavena C, Billaud E, et al. Development of hepatic cytolysis after switching from enfuvirtide to raltegravir in virologically suppressed patients treated with tipranavir/ritonavir. XVII International AIDS Conference. August 3-8, 2008. Mexico City. Abstract TUPE0087.
Recidiva del VHC en personas que consiguieron eliminar el virus al final del tratamiento
Juanse Hernández
En la mañana del jueves, se han presentado diversos estudios sobre la coinfección por VIH y VHC. Un estudio español ha tratado de caracterizar la tasa, el tiempo y los factores pronósticos de recidiva del virus de la hepatitis C en personas coinfectadas que han conseguido aclarar el VHC al final del tratamiento.
Los investigadores del estudio PRESCO inscribieron para este análisis a aquellos participantes que habían recibido tratamiento para la hepatitis C con interferón pegilado alfa-2a y ribavirina (1.000-1.200mg/día) y tenían un nivel de ARN de VHC inferior a 10 UI/ml al finalizar el tratamiento. Se establecieron dos grupos de pacientes: aquéllos que experimentaron una recidiva del VHC después de finalizar el tratamiento –antes de la semana 12 (recidivantes precoces) o antes de la 24 (recidivantes tardíos)–, y aquéllos que consiguieron una respuesta viral sostenida.
En el análisis se incluyó un total de 394 personas, de las cuales 262 (67,3%) tenía carga viral indetectable de la hepatitis C al finalizar el tratamiento (48% con genotipo 1-4 frente a un 90% con genotipo 2-3; p<0,01). En 44 (17%) participantes se produjo recidiva de la hepatitis C: 33 (24%) con genotipos 1-4 y 16 (10%) con genotipos 2-3 (p=0,02).
Los resultados muestran que los genotipos 1-4, carga viral basal igual o superior a 500.000 UI/mL, carga viral del VHC detectable a la semana 4 y uso concomitante de terapia antirretroviral se asociaron con recidiva de la hepatitis C en comparación con las personas que consiguieron una respuesta viral sostenida. Tras finalizar el tratamiento, la recidiva se produjo antes de la semana 12 en 41 personas (84%) –recidivantes precoces– y después de la semana 12, en 8 participantes (16%) –recidivantes tardíos–. La recidiva precoz se dio en un 94% de las personas con genotipo 1-4 y en sólo un 36% de los participantes con genotipo 2-3 (p<0,01). En un individuo con genotipo 3, la recidiva se produjo a la 32 semanas después de finalizar el tratamiento, es decir después de haber conseguido una respuesta viral sostenida a la semana 24.
Según los investigadores, la tasa de recidivas de la hepatitis C en personas coinfectadas por VIH y VHC tratadas con interferón pegilado alfa-2a más ribavirina ajustada al peso es similar a la observada en personas que sólo presentan infección por VHC. Sin embargo, la tasa de personas que recidivan antes de la semana 24 tras finalizar el tratamiento (recidivantes tardíos) podría ser más elevada y común en personas coinfectadas, sobre todo en personas con genotipos 2 y 3.
Fuente: Elaboración propia.
Referencia: Barreiro P, Nuñez M, Santos I et al. HCV relapses upon completion of peg-interferon plus ribavirin in HIV-infected patients: rate, timing and predictors. XVII International AIDS Conference, 3-8 August 2008, Mexico City, abstract THAB0202.
Coinfección y riesgo de infarto agudo de miocardio y enfermedad cerebrovascular
Juanse Hernández
Diversos estudios han mostrado que en las personas coinfectadas por VIH y VHC se observan tasas más bajas de anomalías lipídicas que en personas que sólo están infectadas por VIH. Sin embargo, se desconoce si esto podría afectar a los resultados cardiovasculares en esta población de pacientes. En este sentido, un grupo de investigadores estadounidenses quiso elucidar el impacto de la coinfección por VIH y VHC sobre el desarrollo de enfermedad cardiovascular teniendo en cuenta los tradicionales factores de riesgo cardiaco. Los investigadores compararon los resultados obtenidos con los observados en la etapa anterior a la llegada de la terapia antirretroviral de gran actividad (TARGA, es decir de 1980-1985). Para la era TARGA (1996-2004), se llevaron a cabo análisis de supervivencia para predecir episodios de infarto agudo de miocardio y enfermedad cerebrovascular y se evaluó TARGA como una variable dependiente del tiempo.
Los resultados muestran que la coinfección se asoció con un aumento de la tasa de episodios de infarto agudo de miocardio y de enfermedad cerebrovascular en la etapa anterior a TARGA. En la etapa TARGA, los investigadores analizaron 19.424 personas con VIH, de las cuales un 31,6% estaban coinfectadas por VIH (73.376 paciente-años de seguimiento).
Las tasas de eventos y el cociente de riesgo (CR) ajustado y no ajustado asociado con la coinfección por VHC y controlado por diabetes mellitus, hipertensión, edad y duración de TARGA se detallan en la siguiente tabla:
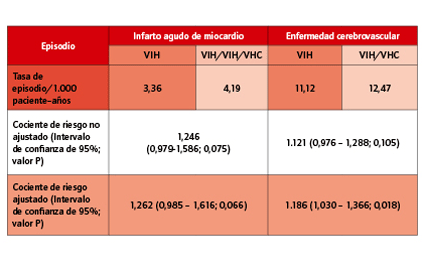
En sus conclusiones los investigadores señalan que la coinfección por VIH se asoció con un incremento significativo de riesgo de infarto agudo de miocardio y de enfermedad cerebrovascular en la etapa anterior a TARGA. En la etapa en la que TARGA ya estuvo disponible, tal efecto parece disminuir por lo que respecta al riesgo de infarto agudo de miocardio, pero el riesgo de enfermedad cerebrovascular continúa siendo elevado.
Fuente: Elaboración propia.
Referencia: Bedimo R, Westfall A, Mugavero et al. HCV co-infection and risk of acute myocardial and cerebrovascular disease among HIV-infected patients in the pre-HAART and HAART eras. XVII International AIDS Conference, 3-8 August 2008, Mexico City, abstract THAB0205.
Darunavir/r tiene un impacto menor sobre los lípidos que lopinavir/r
Xavier Franquet
Darunavir (Prezista®) es un nuevo inhibidor de la proteasa (IP) disponible en España desde 2007 para el tratamiento del VIH en personas con experiencia en tratamientos. La dosis aprobada entonces fue de 600mg dos veces al día junto a 100mg, también dos veces al día, de ritonavir (Norvir®).
Tibotec, el laboratorio que ha desarrollado este fármaco, ha llevado a cabo también un gran estudio en pacientes sin experiencia previa en tratamiento para que este nuevo IP pueda tomarse como parte de una terapia de inicio. Los resultados de este estudio, que recibe el nombre de ARTEMIS, ya fueron presentados el año pasado tanto en la 47 Conferencia Interciencias sobre Agentes Antimicrobianos y Quimioterapia (ICAAC, en sus siglas en inglés) como en la XI Conferencia de la Sociedad Clínica Europea del SIDA (EACS, en sus siglas en inglés) de Madrid (véase La Noticia del Día 26/10/07).
En este ensayo de 48 semanas de duración, darunavir/ritonavir (DRV/r) mostró su no inferioridad al compararse con lopinavir/ritonavir (LPV/r, Kaletra®), acompañados ambos por la combinación de tenofovir más emtricitabina (Truvada®). Los datos ya han sido presentados a las agencias reguladoras y se espera que en breve pueda obtener esta indicación. La dosis que se ha estudiado para esta posible nueva indicación es de 800/100mg de DRV/r una vez al día; y se ha comparado con LPV/r a razón de 800/200mg también una vez al día (aunque en algunos casos se usó la dosis de 400/100mg dos veces al día).
Hoy en la conferencia se ha presentado un póster con datos sobre el impacto en los lípidos de ambos fármacos en combinación con tenofovir más emtricitabina. El análisis arroja resultados favorables a DRV/r que también se asocia a aumentos de los lípidos en sangre, pero en menor medida.
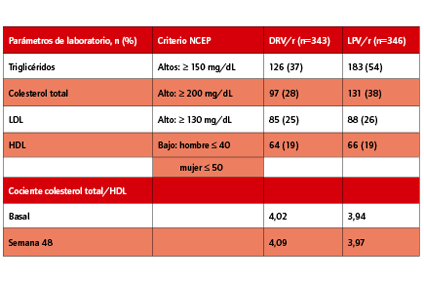
La mayor parte de aumentos fueron leves y moderados (grado 1 y 2) en ambos grupos. En general se dieron con más frecuencia aumentos de colesterol total (33% en el grupo con DRV/r y 45% en el grupo con LPV/r). Los aumentos de moderados a muy graves de colesterol y triglicéridos (grados 2-4) fueron observados con menor frecuencia en el grupo con DRV/r (3% y 13% respectivamente) que en el grupo con LPV/r (11% y 23%, respectivamente).
El porcentaje de pacientes con descensos de colesterol HDL y aumentos de LDL fue similar entre grupos.
Tabla 1: Anomalías de laboratorio surgidas con el tratamiento en la semana 48, según el criterio NCEP
Los autores conluyen que la dosis de 800/100mg de DRV/r una vez al día fue eficaz y se asoció a incrementos menores de triglicéridos y de colesterol total que con el tratamiento con LPV/r.
Fuente: Elaboración propia.
Referencia: Arathoon E, Baraldi E et al. ARTEMIS: lipid tolerability and safety ofa darunavir in antirretroviral-naïve patients. XVII International Conference, 3-8 August, Mexico City, Abstract THPE0151.
Un estudio sobre monoterapia con lopinavir/r muestra altas tasas de fracaso no esperadas
Xavier Franquet
Varios estudios han investigado el tratamiento de monoterapia con lopinavir/r (LPV/r, Kaletra®) y han mostrado que puede mantener la carga viral suprimida durante, al menos, un año. Pero hay pocos datos sobre la actividad de este inhibidor de la proteasa (IP) en ciertos compartimentos, lo que suscita preocupaciones.
Por ello, un grupo de investigadores de la cohorte suiza diseñó un estudio que, con el nombre de MOST, está evaluando la actividad de LPV/r en el tracto genital y en el sistema nervioso central. Se trata de un estudio prospectivo de reparto aleatorio en el que se inscriben pacientes que toman terapia antirretroviral estándar y tienen carga viral indetectable y se reparten en dos grupos para seguir con el tratamiento o pasar a tomar LPV/r en monoterapia. Está previsto que dure 48 semanas y se planeó medir la carga viral en el liquido cefalorraquídeo (LCR) y en las secreciones genitales al inicio y al final del estudio.
De los 58 pacientes que se habían inscrito hasta el momento de elaborar este informe, un total de 23 de 26 en monoterapia y 26 de 28 en terapia estándar habían sido seguidos durante 6 y 12 semanas, respectivamente. Al inicio del estudio todos los pacientes tenían carga viral indetectable. Uno tenía una carga viral de 8 copias/mL en el LCR (fue asignado al grupo de terapia estándar).
En contra de lo esperado, los investigadores observaron numerosos fracasos del tratamiento. Un total de 5 pacientes, todos del grupo con monoterapia, lo experimentó (>400 copias/mL confirmada). Se llevaron a cabo punciones lumbares en tres de ellos y se observó que la carga viral en el LCR era más alta que en sangre. Los cinco confirmaron haber tenido una buena adhesión al tratamiento, pero los niveles de fármaco en sangre eran extremadamente bajos en dos de cuatro.
Tres tenían síntomas neurológicos cuando experimentaron el fracaso (dolor de cabeza, mareos, dificultad de coordinación de movimiento, alteraciones en la visión y dificultad de concentración). Todas las muestras de sangre y LCR eran virus de tipo salvaje según la prueba genotípica.
En sus conclusiones, estos investigadores señalan que la tasa de fracaso con LPV/r podría ser mayor de la esperada e implicar también al sistema nervioso central. Por ello, terminan sugiriendo que el uso de monoterapia con LPV/r se restrinja a los ensayos clínicos.
Estos datos deben interpretarse con suma cautela, pues se trata de un estudio con muy pocos pacientes y con un seguimiento muy corto. De continuar, será interesante comprobar si esta tendencia se mantiene en el tiempo.
Fuente: Elaboración propia.
Referencia: Zenger F, Cusini A et al. Unexpected high failure rate of lopinavir (LPV/r) monotherapy. XVII International Conference, 3-8 August, Mexico City, Abstract LBPE1144.
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.